Dass es eine Verbindung zwischen Allergien und kognitiver Symptomatik gibt, haben viele Allergiker schon bei sich selbst feststellen dürfen. Ein Schub wird oftmals begleitet von Symptomen wie Müdigkeit, Reizbarkeit, Empfindlichkeit, aggressivem Verhalten, die Fähigkeit zum Multitasking nimmt ab, die Konzentrationsfähigkeit ist eingeschränkt bis hin zum gefürchteten Hirnnebel (“brainfog”).
Chronische kognitive Störungen wie Autismus Spektrum Störung (autism spectrum disorder, ASD) und Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) treten auf der anderen Seite häufig assoziiert mit allergischen Erkrankungen, Symptomen und Nahrungsmittelintoleranzen und Verdauungsproblemen auf. Eine Studie zeigte, dass bei 64 % der untersuchten ASD-Patienten gastrointestinale Probleme vorlagen.
Allerdings fallen bei autistischen Kindern Allergietests oftmals negativ aus und es werden keine erhöhten IgE-Werte im Blut gefunden oder Hinweise auf Nahrungsmittelintoleranzen oder Zöliakie, trotz vorhandener Symptome.
Das Problem ist, dass wir viele verschiedene Namen für Allergien und allergieähnliche Symptome haben: Anaphylaxis, Angioödem, Atopie, Atopisches Ekzem, Ausschlag, Asthma, allergische Rhinitis, Heuschnupfen, Nahrungsmittelallergien, Nahrungsmittelintoleranzen, idiopathische Urtikaria, idiopathische Mastzellaktivitätsstörung, Mastozytose, Mastzellaktivierungssyndrom, nicht-IgE vermittelte Nahrungsmittelallergie, Urticaria pigmentosa (Begriffserklärung „idiopathisch“ =„unbekannter Ursache“).
Leider werden ebenfalls oftmals Begriffe wie Nahrungsmittelallergie, -intoleranz, -hypersensitivität zu ungenau eingesetzt, sodass ältere epidemiologische Studien hier keine eindeutigen Daten liefern.
In der Regel verbinden wir mit einer allergischen Reaktion so etwas wie Juckreiz und allergischen Schnupfen, als Reaktion z.B. auf Pollen und Staub. Doch zählen vielleicht auch noch andere Reaktionen dazu, die wir trotz andersartiger Symptomatik ebenfalls zu den Allergien zählen müssten?
All die genannten Reaktionen haben eine Gemeinsamkeit: Sie werden ausgelöst durch Mastzellen. Mastzellen können getriggert werden durch Immunglobuline des Typs E (IgE), aber auch durch eine Vielzahl anderer nicht-allergischer Auslöser wie Verletzungen, Pathogene, Toxine und Stress. Bei Aktivierung entlassen sie ihren Inhalt mit einer Vielzahl an entzündungsfördernden Substanzen. Die Reizdarmsymptomatik kann inzwischen in einigen Fällen ebenfalls einer erhöhten Mastzellaktivität zugeordnet werden, ebenso wie das Leaky-Gut-Syndrom (erhöhte intestinale Permeabilität, durchlässiger Darm).
Weitere ausführliche Infos zu Mastzellen findest du hier!
Die schwerste Mastzellerkrankung ist die Mastozytose, bei der der Körper Mastzellen im Übermaß herstellt. Ein interessanter Fakt ist, dass 1 von 10 Mastozytosepatienten auch die Diagnose ASD hat (wie gesagt, diagnostizierte Fälle, die Zahl kann also noch höher sein)! Die ASD-Prävalenz beträgt etwa 1 von 100, die Mastozytose-Prävalenz nur etwa 1 in 2000 (andere Quellen sprechen von 1 in 4000), es besteht also eine starke Korrelation (bestünde keine Korrelation, wäre die Wahrscheinlichkeit, dass beides zusammen auftritt, bei 1 in 200.000). Kognitive Symptome wie Konzentrationsprobleme, Angststörungen und Verhaltensauffälligkeiten, aber auch schwere psychiatrische Störungen und Epilepsie sind typisch bei Patienten mit Mastozytose, auch ohne ASD-Diagnose. Ebenso typisch sind haut- und gastrointestinale Probleme sowie eine Erhöhung des Serum IL-6-Levels, was ebenfalls typisch ist bei ASD. Das Cytokin IL-6 kann direkten negativen Einfluss auf die Hirnfunktion nehmen.
Zu den möglichen Diagnosekriterien von Mastzellaktivitätssyndrom zählen in zwischen ebenfalls „neurologische Beschwerden“.
Mastzellen kommen nicht nur in unseren Barrieregeweben (die von typischen allergischen Symptomen betroffen sind) wie Haut, Darm, Augen, Nase und Lunge vor, sondern auch im Zentralnervensystem, darunter im Diencephalon („Zwischenhirn“, Teil unseres Gehirns). Besonders der Hypothalamus ist reich an Mastzellen, desweiteren finden wir sie um die Blutgefäße der Blut-Hirn-Schranke reichlich angesiedelt. Der Hypothalamus als wichtigstes Steuerzentrum des vegetativen Nervensystems und der Aufrechterhaltung des inneren Milieus (Homöostase) ist im Grunde der wichtigste Teil unseres Gehirns. Hier laufen zahlreiche neuronale Verbindungen zu anderen Hirnzentren zusammen, wie z.B. zum limbischen System, und es werden wichtige biochemische Regulationen vorgenommen über Hormone, Neuropeptide und biogene Amine wie der Neurotransmitter Dopamin. Ebenso wichtig ist die Blut-Hirn-Schranke, die das empfindliche Gehirn vor Toxinen, Krankheitserregern und Stoffwechselmetaboliten aus unserem restlichen Körper schützt, um eine Aufrechterhaltung der Homöostase zu gewährleisten, die entscheidend ist für eine reibungslose Funktion unserer zentralen Schaltstelle. Störungen in diesen beiden Bereichen können starke Auswirkungen auf den gesamten Organismus haben.
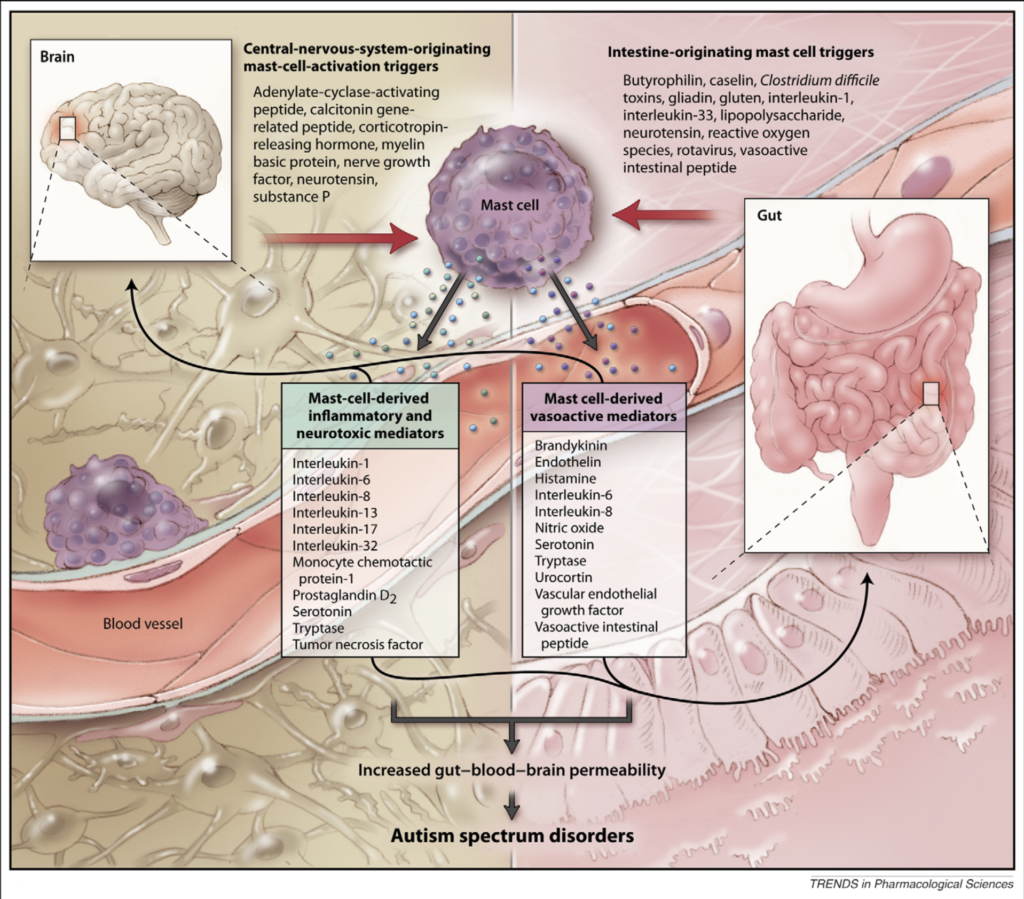
Wie in unseren übrigen Barrieregeweben übernehmen Mastzellen somit auch hier die Funktion der Wächter, der ersten Verteidigungslinie, was seit 1990 bekannt ist. Ansonsten finden wir keine zirkulierenden weißen Blutkörperchen im Gehirn, hier dienen Mikroglia als Immunabwehrzellen. Bei starken Infektionen kann es aber notwendig sein, die Blut-Hirn-Schranke zu öffnen, um zusätzlich Leukozyten aus dem Blutstrom zu rekrutieren, was eine der Aufgaben der Mastzellen ist und über verschiedene vasoaktive Mediatoren (gefäßerweiternde Botenstoffe) geschieht (genau wie im Darm, was dann Leaky-Gut-Syndrom auslöst, siehe Abbildung).
Eine ganze Reihe an Studien zeigen, dass bei ASD (aber auch z.B. bei Multipler Sklerose) eine Störung in der Blut-Hirn-Schranke vorliegt, was durch eine übermäßige Mastzellaktivität hervorgerufen wird. Dies kann zu lokalen entzündlichen Reaktionen im Gehirn führen, die für neuropsychiatrische Symptomatik führt, sowie zum Auftreten von Epilepsie.
Während der Gehirnentwicklung haben wir eine extrem hohe Konzentration an Mastzellen im Gehirn, ca. 4 mal so viele wie bei einem ausgereiften Gehirn. In dieser Zeit ist unser Gehirn demnach deutlich empfindlicher gegenüber Störungen durch Mastzelltrigger!
In unserem Gehirn sowie unserem Darm kommt es zu funktionellen Mastzell-Neuronen-Interaktionen. Immunzellen sind an der Gedächtnisbildung beteiligt durch ihre Fähigkeit, Gewebe zu modellieren. Sie schweißen quasi Nervenzellen um, damit sie neue Synapsen ausbilden können. Mit anderen Worten: Denken und kognitive Arbeit ist entzündungsföderlich (wie Muskelkater)! Wird bei Überreizung von Mastzellen allerdings z.B. ein Übermaß des Enzyms Tryptase ausgestoßen, kann es zum Absterben von Neuronen kommen durch Überaktivierung von Mikrogliazellen, was wir als akuten Brainfog erleben (den wir deshalb nicht auf die leichte Schulter nehmen sollten!).
Auch bei anderen Neuropsychiatrischen Störungen außer ASD konnten diese Interaktionen nachgewiesen werden.
Neueste Entdeckungen zeigen, dass sogar Neuronen Fcε-Rezeptoren (FcεRI) ausbilden können, die bislang nur von Mastzellen und Basophilen (die beiden Zelltypen, die für allergische Reaktionen zuständig sind) bekannt waren. Über den FceRI Rezeptor interagiert Immunglobulin E, das allergische Soforttypreaktionen auslöst, mit diesen Zellen. Allergische Auslöser können somit direkt Neuronen beeinflussen bei Störung der Blut-Hirn-Schranke.
Es ist in dem Zusammenhang interessant zu erwähnen, dass ein paar der älteren Pharmazeutika zur Behandlung von ASD unter anderem auch mastzellblockende Eigenschaften aufweisen. Darüber hinaus gibt es bislang keine effektiven medikamentösen Behandlungsmethoden, Betroffene bekommen meist eine Kombination an verschiedenen Medikamenten verschrieben, ohne dass Kenntnisse zu den Langzeitfolgen bestehen und oft mit erheblichen Nebenwirkungen, ohne Heilungsaussichten.
Mastzellen sind die Hauptproduzenten von Prostaglandinen (Botenstoffe, die aus Arachidonsäure synthetisiert werden). Erhöhte Prostaglandinlevel sind typisch bei ASD-Patienten. Sie sind entzündungsfördernd, gleichzeitig aber auch wichtig für neuronale Plastizität und Gedächtnisbildung. Tumornekrosefaktor wurde ebenfalls als erhöht festgestellt in der Zerebrospinalflüssigkeit vieler Patienten mit ASD-Symptomatik. Hirnmastzellen synthetisieren TNF und sind die einzigen Zelltypen, die präformiertes TNF in ihren Granula speichern können.
Über das Neuropeptid Neurotensin stimulierte Mastzellen können mitochondriale DNA sowie ATP nach außen abgeben, ohne dabei abzusterben. Mitochondrien sind die „Kraftwerke unserer Zellen“, kleine Organellen, die unter anderem ATP herstellen, die Energiewährung unseres Körpers. Diese mitochondrialen Komponenten verstärken, wenn sie außerhalb der Zelle gelangen, allergische oder immunologische Reaktionen (auch z.B. Ekzeme), indem sie wie „angeborene Pathogene“ wirken (Endosymbiontentheorie; die Vorläufer unserer Mitochondrien waren Bakterien). Sie bewirken eine autoentzündliche Reaktion und tragen wahrscheinlich zu der Entstehung von ASD bei. Derselbe Effekt konnte auch bei Schädel-Hirn-Traumata festgestellt werden. Freigesetzte mitochondriale DNA wirkt auch direkt zyto- und neurotoxisch (schädigend für Nervenzellen und andere Zellen) und stellen einen Faktor bei Autoimmunität dar. Bei jungen autistischen Kindern sind entsprechende Werte im Serum erhöht verglichen mit Kontrollprobanden.
Untersuchungen bei Tieren zeigten, dass eine allergische Reaktion zu einer Stimulation des limbischen Systems im Gehirn führt, was zu Vermeidungsstrategien, erhöhter Angst und reduziertem Sozialverhalten führte. Bei Menschen konnte bei einem chronischen allergischen Schub ebenfalls eine veränderte Aktiviät im limbischen System, speziell im anterioren Gyrus cinguli, und dem Präfrontalen Cortex festgestellt werden. Der anteriore Gyrus cinguli ist zuständig für Fehlerfindung, Konfliktmanagment und spielt eine wichtige Rolle in der Verhaltensanpassung. Der Präfrontale Cortex ist wichtig für Planung, Entscheidungsfindung, Motivation und Aufmerksamkeit. Probleme in diesen Bereichen führen zu Aufmerksamkeitsstörungen, Entscheidungsschwierigkeiten, Gedächtnis- und motorischen Problemen und sind typisch bei ADHS und ASD.
Was ergibt sich aus diesen Forschungsergebnissen? Sie zeigen uns, dass auch sogenannte „psychiatrische“ Erkrankungen Ihre Manifestation im Körper finden und der Körper deswegen in der Regel mitbehandelt werden muss (neben z.B. Verhaltenstherapie, die im Grunde aber ebenfalls wieder Einfluss auf unser Gehirn und Bewegungsapparat nimmt). Im Falle von ASD und anderen kognitiven Störungen ist es wichtig, sich auch um den Darm und die allergischen Symptome zu kümmern, um dadurch das Gehirn zu unterstützen. Wie aus meinen bisherigen Artikeln hervorgegangen sein dürfte, bin ich gegen ein Überdecken und Unterdrücken von Symptomen durch Medikamente, z.B. Hydrokortison, SSRIs und Methylphenidat, da unsere Symptome immer Hinweise sind auf ein tiefer liegendes gesundheitliches Problem, welches sich nur verschlimmert, wenn man ihm nicht auf den Grund geht (oxidativer Stress wird sich z.B. nicht nur auf das Gehirn beschränken und ein Mangel an gewissen Nährstoffen, bedingt durch einen geschädigten Darm oder einseitige Ernährung, hat Auswirkungen auf den gesamten Körper). Es wäre, als würde man als einzige Maßnahme bei einem Hausbrand die Batterien aus dem Rauchmelder nehmen. Natürlich müssen je nach Schweregrad gewisse Symptome gelindert werden durch Medikamente wie Antihistaminika, da sie unter Umständen lebensbedrohlich werden können, und Problemstellen behandelt werden, doch der langfristige Weg ist der, einen ganzheitlichen, individualisierten, gesunden Lebensstil anzustreben, bei dem der Körper ins Gleichgewicht finden kann. Hierzu liefere ich viele Ratschläge auf meiner Internetseite.
Die Informationen zu diesem Artikel stammen aus einem Video von Prof. Theoharis C. Theoharides BA, MS, MPhil, PhD, MD – Professor der Pharmakologie, inneren Medizin, Biochemie und Teilprofessur in Psychiatrie, Tufts University, Boston, ausgebildet im Bereich Allergie und klinische Immunologie in Yale – sowie den im Video genannten und weiteren Studien. Prof. Theoharides gehört zu den 5% der am meisten zitierten Autoren wissenschaftlicher Papers und informiert auf seiner Seite über den Zusammenhang zwischen Mastzellen und Autismus. Er glaubt nach all seinen Erfahrungen mit der Arbeit mit autistischen Kindern nicht mehr daran, dass Autismus eine psychiatrische Erkrankung ist.
Mastzellen sind das „Immuntor zum Gehirn“. ~Prof. Theoharis C. Theoharides
Nimm an meinem anschaulichen, leicht verständlichen & gleichzeitig sehr in die Tiefe gehenden Videokurs teil, der die Schnittstelle zwischen Nerven-, Hormon- & Immunsystem erklärt und neue Heilungsansätze eröffnet!
Quellen:
Theoharides, T. C., Tsilioni, I., Patel, A. B., & Doyle, R. (2016). Atopic diseases and inflammation of the brain in the pathogenesis of autism spectrum disorders. Translational Psychiatry, 6(6), e844.
Theoharides, T. C., Asadi, S., Panagiotidou, S., & Weng, Z. (2013). The “missing link” in autoimmunity and autism: extracellular mitochondrial components secreted from activated live mast cells. Autoimmunity reviews, 12(12), 1136-1142.
Lauritzen, K. H., Moldestad, O., Eide, L., Carlsen, H., Nesse, G., Storm, J. F., … & Klungland, A. (2010). Mitochondrial DNA toxicity in forebrain neurons causes apoptosis, neurodegeneration, and impaired behavior. Molecular and cellular biology, 30(6), 1357-1367.
Zhang, B., Angelidou, A., Alysandratos, K. D., Vasiadi, M., Francis, K., Asadi, S., … & Theoharides, T. C. (2010). Mitochondrial DNA and anti-mitochondrial antibodies in serum of autistic children. Journal of neuroinflammation, 7(1), 80.
Rossignol, D. A., & Frye, R. E. (2012). Mitochondrial dysfunction in autism spectrum disorders: a systematic review and meta-analysis. Molecular psychiatry, 17(3), 290-314.
Buske-Kirschbaum, A., Schmitt, J., Plessow, F., Romanos, M., Weidinger, S., & Roessner, V. (2013). Psychoendocrine and psychoneuroimmunological mechanisms in the comorbidity of atopic eczema and attention deficit/hyperactivity disorder. Psychoneuroendocrinology, 38(1), 12-23.
Weissman, J. R., Kelley, R. I., Bauman, M. L., Cohen, B. H., Murray, K. F., Mitchell, R. L., … & Natowicz, M. R. (2008). Mitochondrial disease in autism spectrum disorder patients: a cohort analysis. PloS one, 3(11), e3815.
Theoharides, T. C., Kempuraj, D., & Redwood, L. (2009). Autism: an emerging ‘neuroimmune disorder’in search of therapy. Expert Opinion on Pharmacotherapy, 10(13), 2127-2143.
Dimitriadou, V., Rouleau, A., Tuong, M. T., Newlands, G. J. F., Miller, H. R. P., Luffau, G., … & Garbarg, M. (1997). Functional relationships between sensory nerve fibers and mast cells of dura mater in normal and inflammatory conditions. Neuroscience, 77(3), 829-839.
Rozniecki, J. J., Dimitriadou, V., Lambracht-Hall, M., Pang, X., & Theoharides, T. C. (1999). Morphological and functional demonstration of rat dura mater mast cell–neuron interactions in vitro and in vivo. Brain research, 849(1), 1-15.
Stead, R. H., Dixon, M. F., Bramwell, N. H., Riddell, R. H., & Bienenstock, J. (1989). Mast cells are closely apposed to nerves in the human gastrointestinal mucosa. Gastroenterology, 97(3), 575-585.
De Boer, A. G., & Breimer, D. D. (1998). Cytokines and blood-brain barrier permeability. Progress in brain research, 115, 425-451.
Abbott, N. J. (2000). Inflammatory mediators and modulation of blood–brain barrier permeability. Cellular and molecular neurobiology, 20(2), 131-147.
Theoharides, T. C. (1990). Mast cells: the immune gate to the brain. Life sciences, 46(9), 607-617.
Peachell, P. T., & Pearce, F. L. (1989). Divalent cation dependence of the inhibition by phenothiazines of mediator release from mast cells. British journal of pharmacology, 97(2), 547-555.
Frieling, T., Meis, K., Kolck, U. W., Homann, J., Hülsdonk, A., Haars, U., … & Molderings, G. J. (2011). Evidence for mast cell activation in patients with therapy-resistant irritable bowel syndrome. Zeitschrift für Gastroenterologie, 49(02), 191-194.
Frieling, T., Schemann, M., & Pehl, C. (2011). Das Reizdarmsyndrom–eine Fehlbezeichnung?. Zeitschrift für Gastroenterologie, 49(05), 577-578.
Akin, C., Valent, P., & Metcalfe, D. D. (2010). Mast cell activation syndrome: proposed diagnostic criteria. Journal of Allergy and Clinical Immunology, 126(6), 1099-1104.
Olszewski, M. B., Groot, A. J., Dastych, J., & Knol, E. F. (2007). TNF trafficking to human mast cell granules: mature chain-dependent endocytosis. The Journal
van der Kleij, H., Charles, N., Karimi, K., Mao, Y. K., Foster, J., Janssen, L., … & Bienenstock, J. (2010). Evidence for neuronal expression of functional Fc (epsilon and gamma) receptors. The Journal of allergy and clinical immunology, 125(3), 757.
Theoharides, T. C., Asadi, S., Panagiotidou, S., & Weng, Z. (2013). The “missing link” in autoimmunity and autism: extracellular mitochondrial components secreted from activated live mast cells. Autoimmunity reviews, 12(12), 1136-1142.
Theoharides, T. C., & Zhang, B. (2011). Neuro-inflammation, blood-brain barrier, seizures and autism. Journal of Neuroinflammation, 8(1), 168.
Zhang, Q., Raoof, M., Chen, Y., Sumi, Y., Sursal, T., Junger, W., … & Hauser, C. J. (2010). Circulating mitochondrial DAMPs cause inflammatory responses to injury. Nature, 464(7285), 104-107.

Pingback: Dysautonomie – wenn das vegetative Nervensystem aus dem Gleichgewicht gerät – Philosophie des Gesundwerdens
Pingback: Kein Wunder, dass die Mastzellen… – Philosophie des Gesundwerdens
Pingback: Die 5 Phasen der Heilung des Gehirns – Philosophie des Gesundwerdens
Pingback: Stress als Auslöser für Autismus, ADHS und Neurodermitis – Philosophie des Gesundwerdens
Pingback: Die Rolle von Histamin in der Regulation unserer Emotionen – Philosophie des Gesundwerdens
Pingback: Staub – was auch Nicht-Allergiker wissen sollten – Philosophie des Gesundwerdens
Pingback: Autismus Spektrum Störung, Asthma, Allergien und Umwelttoxine – Philosophie des Gesundwerdens
Pingback: Die große Sehnsucht und die tiefe Angst davor – Philosophie des Gesundwerdens
Pingback: Die chronische Gehirnerschütterung – Philosophie des Gesundwerdens
Pingback: Der biologische Sinn von Trauma – Philosophie des Gesundwerdens
Pingback: Webinareinladung! Was Mastzellmembranen, Haut, Darmflora & Vagusnerv gleichsam natürlich stärkt. – Philosophie des Gesundwerdens